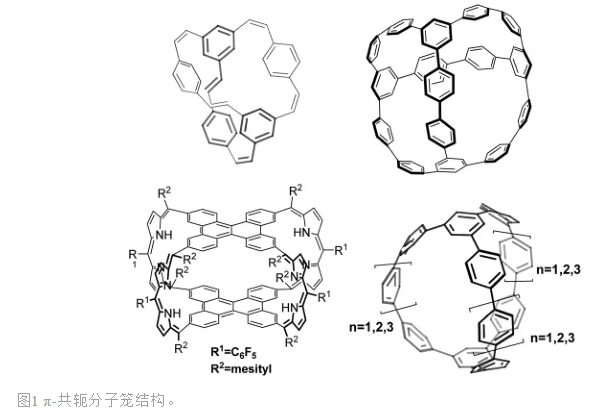
分子笼的合成主要采用超分子组装和动态共价化学方法。然而,由上述方法合成的有机笼(如亚胺,硼酸和二硫化物)存在一些缺点。由于刚性骨架可增强稳定性,我们探索了基于Csp2-Csp2和/或sp杂化碳的分子笼(图1)。稳定笼的合成常用的方法包括不可逆的C-C键形成(如炔烃复分解和过渡金属介导的偶联反应)。然而,存在多步合成、单体单元的预组织、通用方法的缺乏以及总产率较低等问题。因此,开发一种新型共轭分子笼的方法非常重要。π-共轭,卟啉和异卟啉因其电子、光学和电化学性能而被研究。卟啉的这些特性为扩展共轭体系分子的设计提供了可能,可通过沿共轭路径增加原子数量,或通过连接单个大环单元来获得离散的低聚体阵列。
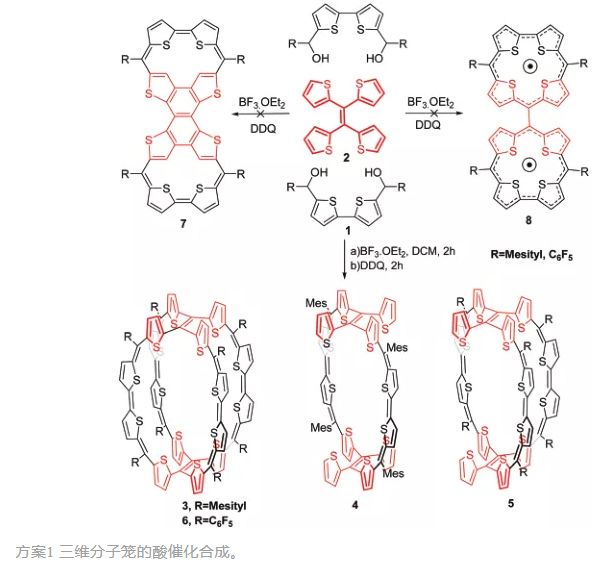
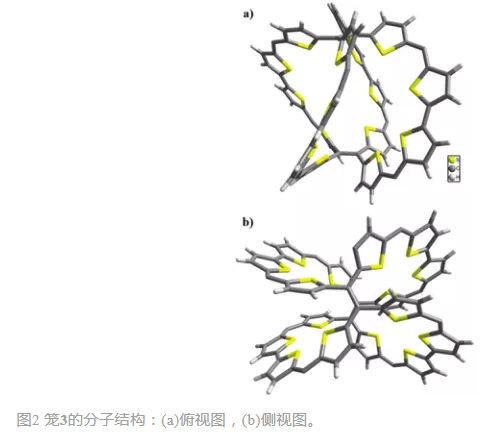
由单晶X射线衍射结构可知(图2),3为三维分子笼,其中四个双噻吩单元(1)与两个四噻吩单元(2)缩合。1作为桥接单元,2作为桥头单元。该笼呈C4对称,所有S原子均朝向笼的中心。与许多卟啉一样,meso甲基取代基与笼状结构接近正交。两个四噻吩乙烯桥头中心间距为9.21 Å,而对角线相对的中间碳原子间距为13.11 Å。该策略被设计用来合成二聚体8,但庞大的噻吩单元对四噻吩大环基团产生了空间位阻。只有噻吩大环或噻吩笼与4nπ异卟啉类非常相似,可如预期进行可逆的环氧化。
由于其共轭网络,3在532 nm 处表现出较大吸收(图3a)。用[Et3O]+[SbCl6]-氧化后,在675 nm处吸收较大值**红移。相比之下,TFA的加入导致在598 nm处的吸收强度相对较低。令人惊讶的是,无论是锌粉,三乙胺或吡啶均不能产生预期的游离碱。这种不可逆的氧化还原是异卟啉的非**现象,因而采用循环伏安法(CV)和光谱电化学测量(图3b)分析了3的不可逆氧化还原机制。CV研究表明,在0.36 V和0.90 V分别发生了两次不可逆氧化,并在-1.21 V出现了还原波。微分脉冲伏安法进一步证实了这些电位。由光谱电化学测量可知,0.4 V在598 nm显示吸收较大值,而在1.1V进一步红移至660 nm (图3 c和d)。这些观察结果表明,TFA 产生单电子氧化自由基阳离子物质,而 Meerwein 盐将分子笼氧化成笼的双阳离子物质 3。然而,化学和电化学氧化还原的不可逆性反映了氧化产物的高度不稳定性。
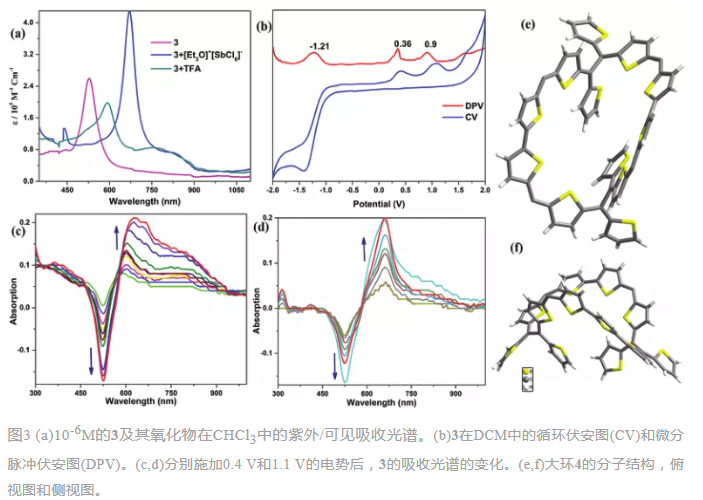
原则上,分子笼可被视为两个40π-八噻吩大环的融合体。然而,由三维结构引起的空间应变使得非平面几何结构减弱了4nπ反芳香性的环电流效应。估算的核独立化学位移(NICS)值为+4.2 ppm,如此低的值清楚地表明三维结构中π电子的弱离域和3的弱反芳香特征。
从该反应中分离出的另一个产物4,由X射线晶体结构可知(图3e和f),其结构为一个大环,其中两个四噻吩单元由两个双噻吩连接。由于共价大环结构中只涉及两个2的噻吩单元,它的另外两个噻吩被发现以反式构象连接在一起,且彼此远离。因此,一个2的噻吩单元指向大环中心,另一个在大环外围。尽管4是一个近二维结构,但它并没有揭示40π反芳香大环**的顺式环电流效应。这可能是由于2的乙烯结的π轨道重叠较差,阻碍了大环结构的全局反芳香性。
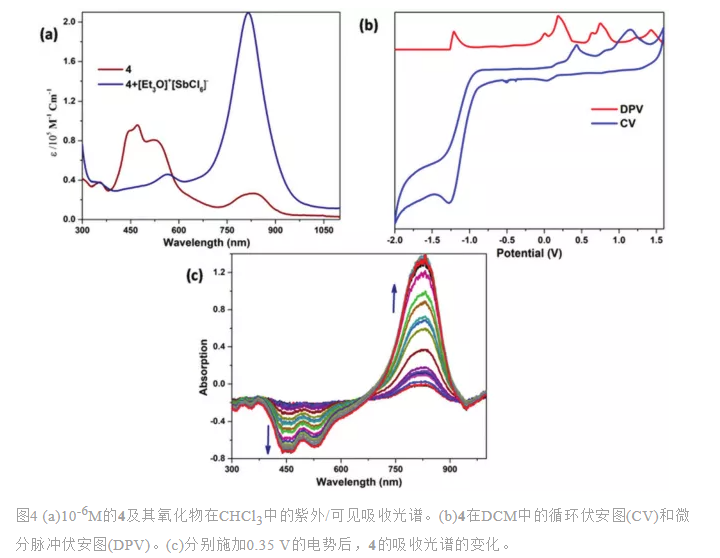
由于扩展的共轭效应,大环4在电磁光谱的可见区域吸收。在443 nm、470 nm和575 nm观察到具有高消光系数的多次吸收(图4a)。作为一个40π体系,4可以预期发生可逆的双电子氧化。因此,添加氧化剂(如Meerwien盐)将吸收较大值转移到825 nm。其强吸收带的吸收系数**增加,红移超过300 nm,表明形成了氧化双阳离子物质。随后,采用循环伏安法(CV)和差分脉冲伏安法(DPV)研究了其电化学性能:该40π大环在+0.014 V和+0.2 V有两个不可逆氧化波,在-1.2 V有一个还原波(图4b)。采用光谱电化学研究所形成的氧化物质 (图4c):在0.35 V(**氧化电位)的作用下,母体的较大吸收峰逐渐消失,并在更高的波长区域(825 nm)出现一个新尖峰。在电氧化吸收光谱中观察到的新峰与化学氧化得到的峰相似。因此,它证实了化学和电化学过程中双阳离子分子的形成。然而,这些双阳离子物质在很长一段时间内都不稳定,可能与它们不稳定的自由基有关。由质谱可知,形成了一个3:2缩合产物5。预计采用囊泡状结构,但由于反应条件不同,产率较低,无法完全表征。


 pg电子娱乐游戏app
微信公众号
pg电子娱乐游戏app
微信公众号 官方微信
官方微信